En doses prophylactiques, la dapsone, un antibiotique de la classe de sulfones, peut-être associée à la méthémoglobinémie et à l’anémie hémolytique chez les patients présentant ou non un déficit en glucose-6-phosphate déshydrogénase (G6PD).
Les facteurs de risque de méthémoglobinémie symptomatique et d’anémie hémolytique incluent la présence sous-jacente d’anémie, de maladie cardiorespiratoire ou de déficit en G6PD.
Il faut soupçonner une méthémoglobinémie en présence de cyanose avec faible saturation en oxygène et pression partielle de l’oxygène normale dans le sang artériel; on obtient la confirmation en mesurant le taux de méthémoglobine.
Le bleu de méthylène est utilisé pour le traitement de la méthémoglobinémie induite par la dapsone, mais il peut être contre-indiqué chez les patients atteints d’hémolyse; la cimétidine est une solution de rechange.
Une femme de 28 ans a consulté aux urgences pour essoufflement et fatigue depuis 4 jours.
La patiente avait reçu un diagnostic de néphropathie à immunoglobulines A (IgA) 1 mois auparavant, après avoir présenté un taux de créatinine de 558 μmol/L (normale 50–110), une protéinurie néphrotique et des résultats d’analyses histologiques à l’avenant à la biopsie rénale. Elle a reçu 3 jours de traitement par méthylprednisolone (1 g/j) puis un cycle dégressif de prednisone orale (débuté à 60 mg/j). On lui a aussi prescrit du triméthoprime–sulfaméthoxazole (800 mg/160 mg PO 3 fois par semaine) en prophylaxie de la pneumonie à Pneumocystis jirovecii. Une éruption cutanée est apparue 12 jours avant la présente consultation et a été attribuée au triméthoprime–sulfaméthoxazole; on lui a alors plutôt prescrit de la dapsone (100 mg/j PO) comme antibiotique de deuxième intention pour la prophylaxie de la pneumonie pneumocystique.
À l’examen, la patiente présentait une cyanose centrale, elle n’était pas en détresse respiratoire et était stable sur le plan hémodynamique. Les examens cardiaques et pulmonaires étaient sans particularités et sa saturation en oxygène était à 89 %–91 % à l’air ambiant et à 91 % sous oxygénothérapie (10 L/min).
Ses résultats d’analyses sanguines étaient comme suit : taux d’hémoglobine à 55 g/L (normale 120–160), volume globulaire moyen à 93,6 fL (normale 80–100), taux de lactate déshydrogénase à 776 UI/L (normale 45–90), taux d’haptoglobine inférieur à 0,10 g/L (normale 0,16–2,20), numération des réticulocytes à 293 × 109/L (normale 25–75) et taux de créatinine à 820 μmol/L (tableau 1). Un frottis sanguin périphérique a montré des érythrocytes fragmentés (figure 1). Les tests de coagulation sanguine, le test de Coombs direct et les électrolytes sériques étaient normaux. Sa radiographie pulmonaire était sans particularités.
Résultats des analyses de laboratoire
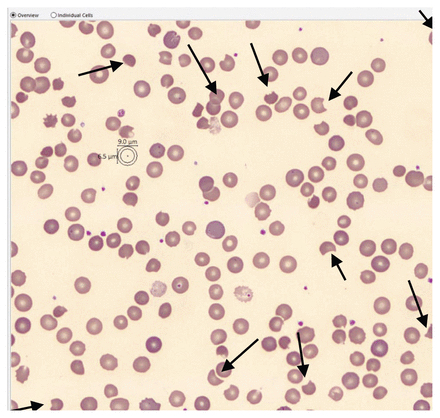
Frottis sanguin prélevé à l’admission à l’hôpital montrant des érythrocytes fragmentés (flèches) qui ont un aspect déformé (bite cell) caractéristique.
L’urgentologue a évoqué une méthémoglobinémie étant donné l’exposition à la dapsone, les faibles taux de saturation en oxygène sans amélioration sous oxygénothérapie et la radiographie pulmonaire normale. L’analyse des gaz veineux a révélé des taux élevés de méthémoglobine à 15,9 % (normale 0,4 %–1,2 %) et des taux normaux de carboxyhémoglobine.
Nous avons consulté l’équipe d’hématologie qui a envisagé un purpura thrombocytopénique thrombotique; toutefois, la numération plaquettaire demeurait stable et l’activité d’ADAMTS13 était normale à 87 % (41 %–130 %). L’équipe a écarté l’anémie hémolytique auto-immune et la coagulation intravasculaire disséminée en raison des résultats normaux aux tests de coagulation sanguine et au test de Coombs. L’absence de symptômes d’infection a permis d’écarter le diagnostic de syndrome urémique hémolytique. À partir des antécédents et des résultats d’analyses de laboratoire, l’équipe d’hématologie a diagnostiqué une probable anémie hémolytique induite par la dapsone et a demandé un dosage de la glucose-6-phosphate déshydrogénase (G6PD).
Après consultation avec le Centre antipoison de l’Ontario, nous avons cessé la dapsone et administré des culots globulaires dans le but d’obtenir un taux d’hémoglobine supérieur à 70 g/L. Nous avons prescrit de la cimétidine orale (300 mg q8h). Nous n’avons pas prescrit de bleu de méthylène, car nous ne connaissions pas le taux de G6PD de la patiente qui, en outre, présentait une hémolyse active et était stable sur le plan clinique.
En accord avec l’équipe d’hématologie, nous avons cessé la cimétidine au jour 3. Au jour 6, les taux de saturation en oxygène de la patiente étaient à 96 % à l’air ambiant et son taux de méthémoglobine avait diminué à 1,6 %. Son taux de G6PD s’est révélé être à 19,4 UI/g Hb (normale 8,3–17,0). Toutefois, l’hémolyse a persisté et des transfusions sanguines ont été requises aux jours 4, 6 et 13. Pendant son hospitalisation, le taux de filtration glomérulaire estimé de la patiente a diminué à 6 mL/min/m2, son œdème périphérique s’est aggravé et elle a dû être placée sous hémodialyse pour son insuffisance rénale terminale due à la néphropathie à IgA. La prednisone utilisée pour traiter la néphropathie à IgA a été graduellement diminuée sur une période de 4 semaines, puis cessée.
La patiente a reçu son congé au jour 13; ses taux de saturation en oxygène étaient alors à 95 %–97 % à l’air ambiant et son taux d’hémoglobine était stable à 72 g/L. Nous avons pu effectuer un suivi lors de ses séances de dialyse 3 fois par semaine. Nous avons commencé l’administration de darbopoïétine (20 μg par semaine par voie sous-cutanée) et de fer par voie intraveineuse pour l’anémie secondaire à l’insuffisance rénale terminale afin d’obtenir un taux d’hémoglobine à 95–115 g/L. Trois mois après son congé, la patiente avait un taux d’hémoglobine à 104 g/L. Un contrôle de la G6PD a révélé une activité normale.
Discussion
La dapsone, un antibiotique de la classe des sulfones qui inhibe la synthèse du folate, est de plus en plus prescrite, surtout pour diverses maladies dermatologiques, y compris la lèpre et la dermatite herpétiforme, mais aussi pour des indications non dermatologiques comme la prophylaxie et le traitement de la pneumonie pneumocystique1.
La pneumonie pneumocystique est une infection opportuniste qui touche les gens immunodéprimés. Peu d’études se sont penchées sur la prophylaxie de la pneumonie pneumocystique chez des patients atteints de maladies auto-immunes ou inflammatoires sous immunosuppresseurs; la prophylaxie de la pneumonie pneumocystique dans ce contexte se fonde donc, pour une bonne part, sur l’opinion des experts.
Chez les patients non infectés par le VIH, la prophylaxie de la pneumonie pneumocystique est suggérée lorsque le risque de pneumonie pneumocystique dépasse 6,2 %, selon une métaanalyse regroupant des patients atteints de cancers hématologiques ou des receveurs d’organes, où le nombre de patients à traiter pour prévenir 1 cas de pneumonie pneumocystique était de 192. La prophylaxie de la pneumonie pneumocystique est suggérée chez les patients sous prednisone (> 20 mg) pendant plus de 1 mois pour des maladies à haut risque, comme la granulomatose avec polyangéite et les maladies des tissus conjonctifs accompagnées d’une maladie pulmonaire interstitielle3. Elle devrait être envisagée chez les patients exposés à des maladies à risque intermédiaire, y compris la vascularite à auto-anticorps cytoplasmiques antineutrophiles et les maladies des tissus conjonctifs avec atteinte rénale3.
Les risques associés à la pneumonie pneumocystique surclassent les risques du traitement prophylactique, puisque cette pneumonie tend à causer une maladie plus grave qui évolue rapidement et menace le pronostic vital chez les patients non infectés par le VIH3. Même si le traitement de première intention est le triméthoprime–sulfaméthoxazole, une revue systématique a révélé que jusqu’à 3 patients sur 100 cessent de prendre le médicament en raison d’effets indésirables tels que la leucopénie, la thrombocytopénie et les éruptions cutanées, comme dans le cas présent2. La dapsone est un traitement de seconde intention qui est utilisé plus souvent, ce qui rappelle l’importance d’en reconnaître les effets indésirables potentiels.
La dapsone atteint sa concentration maximale en 2–6 heures après son ingestion; sa demi-vie est de 20–30 heures4. Elle est métabolisée par acétylation hépatique en ses métabolites inactifs, et par les enzymes du cytochrome P450, qui produisent l’hydroxylamine, son métabolite toxique. Ce dernier subit une recirculation entérohépatique et est rapidement capté par les érythrocytes, ce qui peut entraîner l’hémolyse et la méthémoglobinémie4. Les effets indésirables dépendent généralement de la dose et sont plus susceptibles de provoquer des symptômes chez les patients qui présentent déjà une anémie, une insuffisance cardiorespiratoire ou un déficit en G6PD5.
La méthémoglobinémie est en général due à une exposition à des médicaments, dont la dapsone et la benzocaïne en vaporisateur, à une surdose de nitrate d’amyle ou de nitrite de sodium, à d’autres problèmes de santé, comme le sepsis et la crise d’anémie à hématies falciformes, et, chez les enfants, à la déshydratation6. Selon une étude rétrospective de 2004, la dapsone aurait causé 42 % des cas de méthémoglobinémie acquise (taux moyen de méthémoglobine de 7,6 %), tandis que la benzocaïne en aurait été une cause moins fréquente (20 %), mais entraînant un taux plus élevé de méthémoglobine (43,8 %)6. Selon des données probantes limitées, de 4 %–13 % des patients traités par dapsone viendraient à présenter une anémie hémolytique ou une méthémoglobinémie4. Une étude cas–témoins a mentionné l’hémolyse chez 5,8 % des receveurs de greffes de cellules souches hématopoïétiques recevant la dapsone en prophylaxie, et l’hémolyse avec méthémoglobinémie chez 3,2 % de la cohorte7.
Dans une série de 6 cas traités par dapsone, tous les patients ont présenté des taux élevés de méthémoglobine après 2 semaines de traitement8. Toutefois, les taux de méthémoglobine ne sont pas mesurés d’emblée après le début du traitement par dapsone; on ignore donc l’incidence exacte de la méthémoglobinémie asymptomatique induite par la dapsone. Le déclenchement de la méthémoglobinémie après le début du traitement par dapsone est variable : une étude regroupant 16 patients receveurs d’un organe plein et traités par dapsone en prophylaxie a révélé que la méthémoglobinémie se manifestait après un nombre médian de 48 jours (intervalle 7–809) suivant le début du traitement3. Dans le présent cas, la patiente a consulté 12 jours après le début du traitement par la dapsone.
En général, les taux de méthémoglobine sont supprimés (< 1 % de l’hémoglobine totale) par des enzymes protectrices. Toutefois, lorsque ces enzymes sont trop sollicitées ou dysfonctionnelles, par exemple en présence d’un déficit en G6PD, ou si les érythrocytes sont exposés à un stress oxydatif en raison d’une exposition aux métabolites toxiques de médicaments tels que la dapsone, l’hémoglobine se convertit en méthémoglobine. Et comme la méthémoglobine ne peut pas se lier à l’oxygène, on assiste à une déviation vers la gauche de la courbe de dissociation de l’oxyhémoglobine, qui entraîne une baisse de l’oxygénation des tissus4.
La plus fréquente caractéristique de la méthémoglobinémie est l’hypoxémie réfractaire avec discordance entre les lectures de l’oxymètre de pouls (SpO2) et les taux de saturation en oxygène des gaz artériels (pression partielle de l’oxygène dans le sang artériel, PaO2). La présence de cyanose, des lectures de SpO2 faibles et une PaO2 normale devraient justifier un contrôle de la méthémoglobinémie. La co-oxymétrie est une méthode non effractive de mesure des taux de méthémoglobine. Toutefois, le diagnostic est en général confirmé par l’analyse des gaz sanguins4. Même si un taux de méthémoglobine supérieur à 1 % est anormal, les symptômes n’apparaissent en général qu’à des taux supérieurs à 20 % (tableau 2). Dans ce cas-ci, la patiente souffrait de dyspnée et son taux de méthémoglobine était à 15,9 %; mais son anémie comorbide liée à l’insuffisance rénale terminale a probablement contribué à ses symptômes.
Manifestations cliniques de la méthémoglobinémie selon le taux de méthémoglobine4
Le traitement de la méthémoglobinémie repose principalement sur le bleu de méthylène, qui agit comme cofacteur du système enzymatique de la NADPH–méthémoglobine réductase pour produire le bleu de leucométhylène, qui permet la reconversion de la méthémoglobine en oxyhémoglobine4. Le NADPH requis pour ce processus est généré par les érythrocytes par l’entremise de la G6PD. Lorsque le NADPH diminue, en présence entre autres d’un déficit en G6PD, le bleu de méthylène peut causer une hémolyse. Il peut aussi aggraver l’anémie hémolytique à corps de Heinz induite par la dapsone4. Dans ce cas-ci, sur les conseils du centre antipoison, nous avons choisi de ne pas utiliser le bleu de méthylène en raison du statut inconnu de la G6PD de la patiente, de la présence d’hémolyse et de sa stabilité hémodynamique.
La cimétidine, un anti-H2, est un autre traitement de la méthémoglobinémie induite par la dapsone. Elle entre en concurrence avec la dapsone pour les enzymes du cytochrome P450, abaisse de la production du métabolite toxique, l’hydroxylamine, ce qui réduit le taux de méthémoglobine9,10. Chez notre patiente, nous avons cessé la dapsone et commencé la cimétidine, qui a été maintenue jusqu’au jour 3, lorsque les taux de saturation en oxygène à l’air ambiant ont dépassé 92 %. Une série de cas a révélé que la cimétidine réduisait les taux de méthémoglobine chez les patients sous traitement prolongé par dapsone dans la semaine suivant son début8. Ensemble, l’arrêt de la dapsone et la mise en route de la cimétidine peuvent avoir accéléré la résolution de la méthémoglobinémie chez cette patiente, alors que l’arrêt de la dapsone seul a entraîné la normalisation des taux de saturation en oxygène en l’espace de 24 heures6.
L’hémolyse consécutive à une exposition à la dapsone est liée à la formation de corps de Heinz lorsque le fer hémique est exposé à l’hydroxylamine, le métabolite toxique de la dapsone11. Les corps de Heinz sont ciblés par les macrophages spléniques et créent des hématies déformées caractéristiques, comme chez cette patiente11. Le risque d’hémolyse augmente chez les patients qui ont un déficit en G6PD parce que cette enzyme protège les érythrocytes de la destruction en présence de stresseurs oxydatifs12. Les résultats du dosage initial de la G6PD chez cette patiente étaient normaux; toutefois, l’activité enzymatique peut être normale durant une réaction hémolytique aiguë. Il est suggéré de faire des contrôles de G6PD dans un intervalle d’au moins 2 semaines à 3 mois après la réaction aiguë12. Dans ses lignes directrices pour le diagnostic du déficit en G6PD par analyse de laboratoire, la British Society for Haematology recommande un dépistage systématique du déficit en G6PD chez tout patient qui commence un traitement par dapsone13. Fait à noter, l’hémolyse peut survenir en l’absence de déficit en G6PD, comme ce fut le cas chez notre patiente.
Footnotes
Intérêts concurrents: Aucun déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement de la patiente.
Collaborateurs: Tous les auteurs ont contribué à la conception de ce rapport de cas et à l’acquisition des données. Gabriella Jacob a rédigé l’ébauche du manuscrit. Louise Moist et Melissa Schorr l’ont révisé de façon critique pour confirmer les renseignements sur le cas et le contenu intellectuel le concernant. Toutes ont aussi approuvé la version finale pour publication et accepté d’assumer l’entière responsabilité de tous les aspects du travail.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/