Le syndrome des ovaires polykystiques (SOPK) est une maladie chronique qui s’accompagne d’infertilité, de fausses-couches, d’issues défavorables de la grossesse, et de risques cardiovasculaires, métaboliques, psychologiques et néoplasiques.
Le diagnostic du SOPK peut être posé sur la base de la présence de 2 irrégularités des cycles menstruels, d’une hyperandrogénie clinique ou biochimique ou d’une morphologie des ovaires polykystiques à l’échographie transvaginale.
La prise en charge du SOPK peut cibler l’anovulation, l’excès d’androgènes, l’hyperinsulinémie et la gestion du poids.
Les personnes atteintes du SOPK devraient se soumettre à un suivi rigoureux de leur indice de masse corporelle, de leur tension artérielle et de leurs paramètres métaboliques, et devraient faire l’objet d’un dépistage périodique de la dépression, de l’anxiété et de l’apnée obstructive du sommeil.
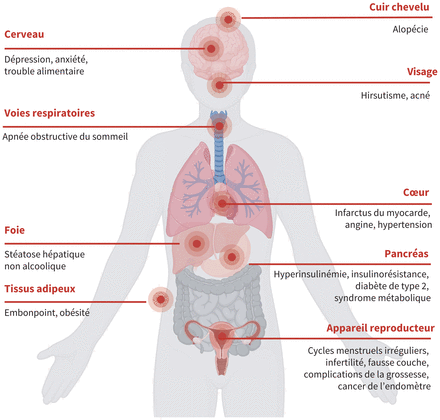
Le syndrome des ovaires polykystiques (SOPK) s’accompagne d’une irrégularité des cycles menstruels et de symptômes d’hyperandrogénie; il affecte 10 % des femmes (figure 1)1. Le plus souvent, les symptômes se manifestent entre les âges de 18 et 39 ans, mais le diagnostic et le traitement tardent souvent ou alors les cas restent non diagnostiqués1,2. Les personnes atteintes de SOPK sont plus susceptibles de souffrir d’embonpoint ou d’obésité (53 %–74 %) que les personnes indemnes et un indice de masse corporelle (IMC) élevé est associé à des symptômes de SOPK plus graves3–5. Les personnes qui présentent un SOPK ont aussi des taux plus élevés de complications aux plans reproducteur, cardiovasculaire, psychologique, métabolique et néoplasique comparativement à la population féminine générale3,6. Un diagnostic précoce de SOPK permet d’identifier et de traiter les problèmes de santé associés, comme l’hypertension, le diabète, l’apnée obstructive du sommeil, la dépression et l’anxiété. Nous passons ici en revue les données probantes sur la physiopathologie, le diagnostic et la prise en charge du SOPK tirées de lignes directrices et d’autres articles pertinents (encadré 1).
Incidences du syndrome des ovaires polykystiques sur la santé. Créé à l’aide de BioRender.com.
Encadré 1: Données probantes employées dans la présente revue
Nous avons consulté la ligne directrice internationale pour la prise en charge du syndrome des ovaires polykystiques (SOPK) publiée en 2023 par la Société européenne de reproduction humaine et d’embryologie et la Société américaine de médecine reproductive et la ligne directrice sur l’hirsutisme publiée en 2018 par la Société d’endocrinologie1,3,7. Nous avons aussi recherché les articles pertinents sur PubMed de 2018–2023 à partir des termes anglais « PCOS » et « polycystic ovarian syndrome ». Nous avons tenu compte de tous les articles et exploré les listes bibliographiques des articles pertinents pour y trouver d’autres sources intéressantes.
Quelle est la physiopathologie du SOPK?
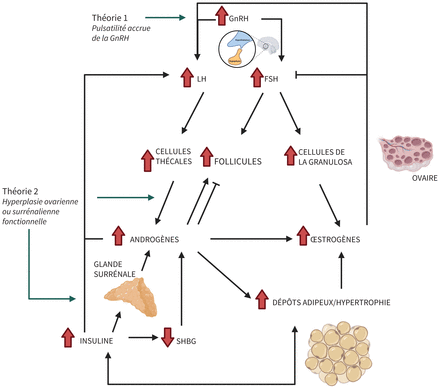
La physiopathologie du SOPK est complexe et encore mal comprise. L’hyperandrogénie et l’hyperinsulinémie sont au cœur des symptômes cliniques, du diagnostic et des objectifs thérapeutiques du SOPK. Les phénotypes cliniques varient grandement. Il reste à déterminer si la présence de follicules ovariens immatures, caractéristiques du SOPK, précède l’hyperandrogénie, l’hyperinsulinémie et leurs symptômes cliniques associés, ou si c’est l’inverse qui se produit (figure 2)8.
Il y a 2 théories pour expliquer la physiopathologie du syndrome des ovaires polykystiques (SOPK). Les 2 mécanismes physiopathologiques principaux qui définissent le SOPK sont l’hyperandrogénie et l’hyperinsulinémie; ce lien a été décrit et ils contribuent mutuellement à se perpétuer, mais le mécanisme exact n’a pas été entièrement élucidé. Les 2 principales théories avancées incluent l’augmentation de la sécrétion pulsatile de la gonadolibérine (GnRH) (théorie 1) et hyperandrogénie ovarienne ou surrénalienne fonctionnelle (théorie 2). La gonadolibérine stimule la sécrétion de folliculostimuline (FSH) et d’hormone lutéinisante (LH) à partir de l’hypophyse antérieure. Dans l’ovaire, la LH influe sur la sécrétion d’androgènes par les cellules thécales; la FSH agit sur la granulosa qui produit des œstrogènes. Les œstrogènes ont des mécanismes de rétroaction négative sur la production de FSH. Les androgènes et les œstrogènes stimulent la production de LH. La sécrétion ovarienne d’androgènes peut aussi être fonctionnelle. L’hyperandrogénie, de même que la stimulation par la FSH et la LH, accélèrent le développement folliculaire et l’atrésie responsables de l’aspect multifolliculaire classique des ovaires à l’échographie. Les androgènes peuvent aussi être produits en excès par les surrénales, phénomène parfois amplifié par l’insuline. L’hyperinsulinémie et l’hyperandrogénie seraient aggravées par les dépôts de tissus adipeux et pourraient également en être la cause. Créé à l’aide de BioRender.com. Remarque: SHBG = globuline liant les hormones sexuelles.
Deux théories ont été avancées pour expliquer l’hyperandrogénie qui accompagne le SOPK8. Selon la première théorie, appelée théorie de la sécrétion altérée des gonadotrophines, l’augmentation de la fréquence de sécrétion pulsatile de la gonadolibérine (GnRH) donne lieu à des taux excessifs d’hormone lutéinisante (LH) et à des taux légèrement élevés de folliculostimuline (FSH)9–11. La hausse des taux de LH stimule la production androgénique à partir des cellules thécales, tandis qu’une FSH élevée favorise le développement folliculaire et une production excédentaire d’œstrogènes10,11. Selon la seconde théorie, appelée théorie de l’hyperandrogénie ovarienne ou surrénalienne fonctionnelle, l’hyperandrogénie provient d’un dérèglement de la stéroïdogenèse au niveau des ovaires ou des surrénales8.
L’élévation des androgènes favorise le recrutement des follicules tout en induisant leur atrésie8,10,12, responsables de l’aspect typique des ovaires multifolliculaires (ou polykystiques) à l’échographie transvaginale.
L’hyperinsulinémie exercerait de multiples effets, y compris une élévation de la LH, une baisse de la globuline liant les hormones sexuelles (SHBG), une conversion accrue de l’androstènedione en testostérone et une réduction de la désensibilisation à la LH au niveau de l’ovaire9,10. L’hyperinsulinémie entraîne une augmentation des dépôts de tissus adipeux viscéraux et leur hypertrophie. L’hyperandrogénie peut aussi mener à une adiposité viscérale accrue. L’obésité aggrave les symptômes de SOPK, mais la prévalence de ce dernier n’augmente que légèrement en proportion de l’IMC, ce qui laisse entendre que l’obésité ne serait pas la principale cause du SOPK5,10,13.
Comment les personnes décrivent-elles leurs symptômes de SOPK?
Le SOPK s’accompagne souvent d’une irrégularité des cycles menstruels avec ou sans caractéristiques d’hyperandrogénie, qui incluent l’hirsutisme, l’acné et une alopécie féminine (chevelure éclaircie, mais préservation de la ligne capillaire)1. Avant de pouvoir poser un diagnostic de SOPK, d’autres causes de ces phénomènes doivent d’abord être écartées. Ces autres causes incluent l’hyperprolactinémie, la dysfonction thyroïdienne, l’hyperplasie surrénalienne congénitale non classique, le syndrome de Cushing, les tumeurs ovariennes et les tumeurs surrénales. Une anamnèse détaillée est la première étape qui permet de faire la distinction entre les diverses causes potentielles des symptômes.
Symptômes évocateurs d’un SOPK
Le SOPK s’accompagne typiquement d’une irrégularité des cycles menstruels, qui va parfois de pair avec une anovulation. Dans les cas de SOPK, les règles peuvent fluctuer tout au long de la vie entre aménorrhée et cycles ovulatoires réguliers. Les médecins doivent déterminer si la personne a des antécédents familiaux de SOPK, de dyslipidémie, d’hypertension ou de diabète, étant donné que le SOPK a une composante héréditaire3.
Les symptômes androgéniques du SOPK, comme l’acné, l’hirsutisme et l’alopécie féminine, s’installent graduellement. L’hirsutisme, qui est le symptôme le plus prédictif d’une hyperandrogénie biochimique, peut être évalué objectivement au moyen du score de Ferriman et Gallwey, même si l’utilité clinique de ce système de classification est limitée du fait que les personnes procéderont souvent à une épilation avant d’être examinées1. Ainsi, une croissance pileuse subjective qui cause une détresse peut suffire pour envisager un traitement1.
Caractéristiques cliniques évocatrices d’autres diagnostics
D’autres causes de l’hyperandrogénie et de l’irrégularité du cycle menstruel peuvent ressembler au SOPK, notamment l’hyperplasie congénitale des surrénales non classique et le syndrome de Cushing. Tandis que l’hyperplasie congénitale des surrénales non classique est cliniquement indifférenciable du SOPK, quant à lui, le syndrome de Cushing s’accompagnera d’autres caractéristiques telles que stries violacées, gain pondéral avec dépôts de graisse abdominale et coussinets adipeux dorsaux, ecchymoses au moindre choc et faiblesse des muscles proximaux.
Les saignements intermenstruels et les règles abondantes ne sont généralement pas associés au SOPK; il faut envisager des causes infectieuses ou structurelles en présence de saignements abondants, telles que fibromes, polypes ou adénomyose. Les symptômes associés, notamment les bouffées de chaleur dans le contexte d’une irrégularité récente des cycles menstruels, sont plus évocateurs d’une insuffisance ovarienne prématurée.
En présence de dysfonction thyroïdienne et d’hyperprolactinémie, d’autres symptômes peuvent s’ajouter; des anomalies de la peau ou des phanères ou une sensibilité au chaud ou au froid accompagnent souvent la dysfonction thyroïdienne, alors que la galactorrhée, les céphalées, les troubles visuels sont caractéristiques d’une hyperprolactinémie. Une revue complète des médicaments susceptibles de causer l’hyperprolactinémie ou l’hyperandrogénie s’impose donc également. Le déclenchement soudain de symptômes graves de virilisation (p. ex., clitoromégalie, voix plus grave, alopécie masculine) évoque davantage une tumeur surrénalienne ou ovarienne sécrétant des androgènes7.
Comment diagnostique-t-on le SOPK?
Les critères de Rotterdam sont les plus largement acceptés pour le diagnostic du SOPK (encadré 2)1. Étant donné que le SOPK est considéré comme un diagnostic d’exclusion, il faut procéder à des épreuves diagnostiques en présence de symptômes, même si les résultats sont parfois normaux. Les analyses suggérées sont présentées dans l’encadré 3, et le tableau 1 propose une interprétation de leurs résultats. En présence de maladie concomitante, comme l’hypothyroïdie, il faut d’abord traiter cette dernière, après quoi on réévalue pour confirmer qu’il s’agit bien d’un SOPK.
Encadré 2: Critères de Rotterdam1
Le diagnostic de syndrome des ovaires polykystiques peut être posé lorsque 2 des 3 critères suivants sont réunis et que les autres diagnostics ont été écartés:
Cycles irréguliers (si > 3 ans post-ménarche, intervalle > 35 j ou < 21 j; < 8 cycles menstruels par année; ou tout cycle > 90 j)
Hyperandrogénie clinique (acné, hirsutisme, alopécie) ou biochimique
Morphologie des ovaires polykystiques à l’échographie transvaginale ou taux élevé d’hormone antimüllérienne*
↵* Ne s’applique que si la personne a ses règles depuis au moins 8 ans.
Encadré 3: Analyses initiales suggérées en présence de cycles menstruels irréguliers ou d’hyperandrogénie clinique
Les analyses devraient être effectuées durant la phase folliculaire précoce (jours 2–4) chez les personnes non aménorrhéiques
Prolactine
Thyréostimuline
Hormone lutéinisante, folliculostimuline et estradiol
Gonadotrophine chorionique humaine β (β-hCG)
17-hydroxyprogestérone (17-OHP)
Testostérone totale, testostérone libre calculée ou indice d’androgènes libres avec ou sans androstènedione, sulfate de déhydroépiandrostérone
Échographie transvaginale ou taux d’hormone antimüllérienne*
↵* Facultatif si les critères cliniques ne sont pas réunis; l’hormone antimüllérienne est utilisée comme solution de rechange à l’échographie transvaginale, mais ne devrait pas être utilisée à l’adolescence.
Analyses initiales et diagnostics différentiels du syndrome des ovaires polykystiques
L’hyperandrogénie biochimique s’observe dans 60 % des cas de SOPK et peut être évaluée en mesurant les taux de testostérone totale, de testostérone libre calculée, de sulfate de déhydroépiandrostérone (DHEA S) et d’androstènedione1. Si possible, on effectuera le dosage de ces androgènes de façon séquentielle en commençant par la testostérone totale et la testostérone libre calculée ou l’indice d’androgènes libres. Si ces analyses initiales sont normales, on mesure ensuite les taux de DHEA S et d’androstènedione1. Les taux d’androgènes ne sont qu’accessoirement élevés en présence de SOPK: toute élévation marquée devrait conduire à un dépistage plus ciblé de tumeurs sécrétant des androgènes1. Les taux d’androgènes ne peuvent pas être mesurés de manière fiable si la personne prend des contraceptifs hormonaux d’association (CHA) parce que l’élévation de la SHGB et l’altération de la sécrétion androgénique dépendante des gonadotrophines faussent les résultats à la baisse1. Si la personne présente 2 critères de Rotterdam sur 3, cela suffit pour poser un diagnostic de SOPK sans analyses pour confirmer une hausse des androgènes. Si une confirmation en laboratoire est nécessaire, les CHA doivent être cessés 3 mois avant le dosage des androgènes16.
La morphologie des ovaires polykystiques à l’échographie transvaginale (≥ 20 follicules ou volume de l’un des 2 ovaires ≥ 10 mL) serait un critère additionnel si les critères cliniques ou les analyses de laboratoires ne concordent pas1,12,17. Une échographie transabdominale peut être utilisée comme solution de rechange avec des seuils différents (≥ 10 follicules ou volume de l’un des 2 ovaires ≥ 10 mL)1. La requête doit mentionner un diagnostic clinique possible de SOPK pour qu’une numération des follicules excédentaires soit effectuée. Le nombre normal de follicules par ovaire peut se recouper selon l’âge et la morphologie des ovaires polykystiques; le nombre normal moyen de follicules est de 8 chez les femmes en âge de procréer, avec un volume moyen de 6,1 mL1,18. On peut observer une morphologie d’ovaires polykystiques chez jusqu’à 25 % des femmes en bonne santé et cela est considéré comme une variante de la normale19. Il faut informer les personnes que les kystes sont des follicules immatures présents normalement dans tous les ovaires; c’est le nombre de follicules qui détermine la morphologie des ovaires polykystiques. La découverte fortuite d’une morphologie d’ovaires polykystiques devrait amener les médecins à poser des questions sur la régularité des menstruations, l’acné, l’hirsutisme et l’alopécie, et des analyses de laboratoire ciblées devraient aussi être envisagées pour détecter une hyperandrogénie biochimique.
Le taux d’hormones antimüllériennes est aussi un marqueur du nombre de follicules. Une méta-analyse récente laisse entendre qu’un seuil de diagnostic approprié pour le de SOPK serait un taux d’hormones antimüllériennes de 34,2 pmol/L15. Les valeurs et les seuils dépendent étroitement de l’âge et des résultats d’analyses1. Même si le taux d’hormones antimüllériennes peut être utilisé pour remplacer l’échographie transvaginale, elle est peu accessible dans les laboratoires au Canada et n’est pas remboursée par la plupart des régimes d’assurance maladie provinciaux.
Comment gère-t-on les manifestations cliniques du SOPK?
Le SOPK requiert souvent un traitement pour régulariser les cycles menstruels, réduire l’abondance des règles, atténuer l’acné ou l’hirsutisme et gérer le poids (tableau 2).
Perte de poids
En présence d’embonpoint ou d’obésité, une perte de poids de 5 %–10 % peut aider à atténuer la gravité des symptômes, y compris l’irrégularité des cycles menstruels, l’acné, l’hirsutisme et l’alopécie16,22. Aucune recommandation n’a été formulée quant à un régime alimentaire ou un programme d’exercices spécifique pour le SOPK et les médecins doivent être particulièrement sensibles à la stigmatisation liée au poids, car les personnes atteintes de SOPK risquent de souffrir de dysmorphie corporelle ou de troubles alimentaires1.
Contraceptifs hormonaux d’association
Les contraceptifs hormonaux d’association (CHA) sont l’option pharmacologique de première intention pour régulariser les cycles menstruels et traiter l’hirsutisme ou l’acné. Rien n’indique qu’un type de CHA soit supérieur à un autre pour ce qui est de soulager les symptômes; les lignes directrices ne peuvent donc pas en préconiser un en particulier1,7. Le traitement de l’hyperandrogénie au moyen des CHA repose sur plusieurs mécanismes; la composante œstrogénique influe à la hausse sur la SHBG, ce qui réduit la quantité de testostérone libre, et les œstrogènes et progestatifs ont des mécanismes de rétroaction négative qui agissent sur la sécrétion hypophysaire de LH et réduisent ainsi la production d’androgènes ovariens induite par la LH23.
Plusieurs personnes souhaitent spécifiquement avoir un cycle régulier, même si cela n’est pas médicalement nécessaire dans la mesure où les cycles se répètent à moins de 90 jours d’intervalle. L’irrégularité des cycles peut être associée à des saignements abondants. Les contraceptifs hormonaux d’association sont des agents de première intention qui rendent les règles prévisibles. Lorsque les œstrogènes sont contre-indiqués ou non tolérés, les modalités exclusivement progestatives incluent les progestatifs oraux et injectables, les dispositifs intra-utérins à libération de lévonorgestrel et les implants sous-cutanés d’étonogestrel. Les progestatifs oraux peuvent être utilisés de façon cyclique (c.-à-d., 3 semaines sur 4) ou plus ponctuelle (c.-à-d., traitement court après > 90 j d’aménorrhée) pour régulariser les règles. L’utilisation continue de progestatifs entraînera probablement l’aménorrhée. Il faut rassurer les personnes en leur disant qu’il s’agit d’un effet normal du médicament, à ne pas confondre avec l’oligoménorrhée associée à un SOPK non traité. Les dispositifs intra-utérins à libération de lévonorgestrel et les implants souscutanés d’étonogestrel peuvent offrir aux personnes une protection endométriale et réduire les douleurs et les saignements menstruels, mais ne permettent pas de rendre les règles prévisibles. Plusieurs progestatifs exercent une forte activité androgénique et peuvent aggraver l’hyperandrogénie clinique7.
Quand l’aménorrhée dure plus de 90 jours, une protection endométriale est cruciale. Le risque de cancer de l’endomètre est 2–6 fois plus élevé chez les personnes atteintes de SOPK que chez la population générale et s’observe souvent avant la ménopause1. Dans les cas d’aménorrhée prolongée, il faut offrir des CHA ou des progestatifs pour maintenir la paroi endométriale en phase non proliférative (tableau 2). Une biopsie de l’endomètre est à envisager dès que l’aménorrhée excède 90 jours, surtout si cela survient fréquemment24.
Médicaments non hormonaux
Il arrive que les CHA soient contre-indiqués ou que les personnes préfèrent ne pas prendre d’agents hormonaux. La metformine, qui augmente la sensibilité à l’insuline, peut être utilisée comme solution de rechange non hormonale pour le SOPK en favorisant une modeste perte pondérale et en réduisant les taux d’insuline, ce qui peut avoir une incidence sur la régularité des cycles et l’hyperandrogénie1. Une méta-analyse de 22 essais randomisés contrôlés (ERC) sur la metformine pour le traitement du SOPK a fait état d’une réduction de l’IMC (−0,53), de la testostérone (−13,36 ng/dL) et de la glycémie à jeun (−2,39 mg/dL)1. Les analyses de sous-groupes ont démontré que la metformine faisait diminuer l’IMC, la glycémie à jeun et les taux de lipoprotéines totales et de basse densité en présence d’IMC supérieurs à 25, alors que l’indice d’androgènes libres et l’insuline à jeun diminuaient en présence d’un IMC égal ou inférieur à 251. L’efficacité de la metformine pour les symptômes cliniques du SOPK reste incertaine. Toutefois, étant donné les améliorations des marqueurs métaboliques, on pourrait envisager la metformine dans les cas de SOPK associés à un IMC supérieur à 251.
La metformine a été comparée aux CHA dans le cadre de 22 ERC1. Il n’y a pas de différence statistiquement significative entre les 2 traitements en ce qui a trait au poids, à l’IMC ou à l’hirsutisme selon des données de très faible degré de certitude. Comparativement à la metformine, les CHA ont amélioré significativement l’irrégularité des cycles selon un degré de certitude moyen des données. Comparativement aux CHA, la metformine a amélioré les taux d’insuline et de cholestérol selon des données de très faible degré de certitude1. L’ajout de metformine aux CHA peut être envisagé dans les cas de SOPK à risque métabolique élevé, ce qui inclut IMC supérieur à 30, intolérance au glucose, appartenance à un groupe ethnique présentant des facteurs de risque métabolique élevé et autres facteurs de risque de diabète1.
L’inositol est un supplément en vente libre envisageable pour la prise en charge du SOPK. Il appartient au groupe des vitamines du complexe B et participe à de nombreuses voies de signalisation, entre autres en aval de la FSH et de l’insuline. Il pourrait jouer un rôle dans l’amélioration de la sensibilité à l’insuline1,20. Selon une récente méta-analyse, l’inositol, en particulier le myoinositol, a permis de réduire l’IMC (différence moyenne 0,45 kg/m2) comparativement au placebo20. La normalisation des cycles a été plus marquée dans le groupe sous inositol (risque relatif [RR] 1,79). Le myo-inositol a des effets indésirables minimes, même s’il faudra procéder à d’autres études pour confirmer cela. En outre, étant donné que l’inositol est un supplément, aucune régulation ne s’applique à sa mise en vente libre et il faut par conséquent l’utiliser avec prudence1,20.
Agents antiandrogéniques
Les agents antiandrogéniques peuvent être envisagés en présence d’une hyperandrogénie clinique qui persiste après 6 mois de CHA sans amélioration, ou en présence de contreindications aux CHA. Le traitement médicamenteux de l’hirsutisme permet de prévenir l’apparition de nouvelle pilosité, mais ne peut inverser la pilosité déjà établie7. Seules les techniques d’épilation externe, comme l’épilation au laser photomécanique ou à la lumière pulsée, permettent d’éliminer la pilosité déjà établie. L’ajout d’éflornithine topique peut améliorer les résultats de l’épilation au laser photomécanique ou à la lumière pulsée7.
La metformine et l’inositol peuvent aussi indirectement réduire les taux d’androgènes, même si leur effet spécifique sur la réduction clinique de l’hirsutisme et de l’acné n’a pas encore été démontré1. Les agents antiandrogéniques comme la spironolactone, l’acétate de cyprotérone et le finastéride doivent être utilisés avec une contraception efficace en raison de leur tératogénicité; selon des données probantes, on peut aussi réduire l’hirsutisme en ajoutant des anti-androgènes aux CHA1.
Quels sont les enjeux liés à la fertilité et à la grossesse en présence de SOPK?
Si la personne veut concevoir, les médecins doivent lui rappeler que des cycles irréguliers ou prolongés (> 35 j) peuvent encore être sporadiquement ovulatoires25. La contraception est donc requise si la personne ne souhaite pas concevoir. Et il faut en moyenne plus de temps pour que la personne devienne enceinte; selon une volumineuse étude de population menée en Suède, la conception spontanée prenait en moyenne 2 années de plus chez les personnes atteintes de SOPK26. La fonction ovulatoire et donc la régularité des cycles ont tendance à s’améliorer avec l’âge, même s’il faut toujours prévoir un déclin de la fertilité liée à l’âge, indépendamment du SOPK27.
Dans cette étude suédoise, la probabilité cumulative de donner naissance après une fécondation naturelle a été de 55 % chez les personnes atteintes de SOPK, contre 73,8 % chez les femmes indemnes26. Avec la procréation assistée, la probabilité cumulative de donner naissance a été la même chez les personnes atteintes de SOPK (80 %) et les personnes indemnes (78 %)26. Les options de première intention qui peuvent être instaurées par les médecins de soins primaires pour gérer le retour aux cycles ovulatoires incluent perte de poids de 5 %–10 % en présence d’embonpoint ou d’obésité, metformine, inositol ou létrozole1. Il est envisageable d’essayer ces méthodes pendant 6–12 mois chez les personnes de moins de 35 ans. La metformine et l’inositol sont sécuritaires durant la grossesse; toutefois, sauf si la personne souffre également de diabète de type 2, aucune donnée concluante n’en appuie le maintien durant la grossesse. On peut envisager une demande de consultation auprès de spécialistes de la fertilité en tout temps pour l’induction de l’ovulation au moyen de létrozole, de gonadotrophines ou de forage ovarien laparoscopique (c.-à-d., perforation du cortex ovarien à l’aide d’une aiguille monopolaire)1.
Les personnes enceintes atteintes de SOPK sont exposées à un risque accru de fausse-couche, de gain pondéral gestationnel, de diabète de grossesse, d’hypertension, de pré-éclampsie, de retard de croissance intra-utérine, de prématurité et d’accouchement par césarienne; certains risques peuvent être atténués par le maintien d’un IMC normal1. Étant donné la contribution connue du SOPK au dérèglement glycémique, un dépistage de l’hyperglycémie à jeun et de l’intolérance au glucose au moyen d’un test d’hyperglycémie provoquée par voie orale de 75 g de glucose doit être envisagé avant la conception3. Si ce test n’est pas effectué avant la conception, il faut le faire lors de la première visite prénatale avant la 20e semaine de gestation et à nouveau à 24–28 semaines de gestation1. Même si la qualité des données est faible, le test d’hyperglycémie provoquée par voie orale est la méthode à privilégier pour reconnaître l’insulinorésistance chez les personnes atteintes de SOPK1.
Quelles sont les complications médicales à long terme du SOPK?
Les complications à long terme suivantes ont toutes été associées au SOPK: hypertension, intolérance au glucose, diabète de type 2, syndrome métabolique, stéatose hépatique non alcoolique, dépression, anxiété, apnée obstructive du sommeil et maladie cardiovasculaire (c.-à-d., maladie cardiaque ischémique, infarctus du myocarde et mortalité cardiovasculaire) 16. Ces problèmes de santé ont tendance à survenir plus tôt chez les personnes atteintes de SOPK que chez les témoins appariés selon l’âge27. Les personnes atteintes de SOPK ayant un IMC supérieur à 25 sont exposées à un risque plus élevé de complications médicales à long terme comparativement à celles dont l’IMC est égal ou inférieur à 25. Le suivi médical est souvent fragmenté étant donné qu’on risque de mettre davantage l’accent sur la reproduction que sur les séquelles à long terme28. Les évaluations de départ et de suivi décrites dans l’encadré 4 s’imposent pour toutes les personnes atteintes de SOPK.
Encadré 4: Examen médical au départ et annuellement chez toutes les personnes atteintes de SOPK
Taille, poids et indice de masse corporelle
Tension artérielle
Évaluation du risque cardiovasculaire, y compris tabagisme, activité physique et antécédents familiaux de maladie cardiovasculaire précoce
Bilan lipidique (cholestérol, lipoprotéines de basse densité, lipoprotéines de haute densité et triglycérides)
Statut glycémique, idéalement par test d’hyperglycémie provoquée par voie orale
Dépistage de l’apnée obstructive du sommeil (c.-à-d., ronflements et fatigue au réveil, somnolence ou fatigue diurne)
Dépistage de la dépression et de l’anxiété
Dépistage de toute aménorrhée excédant 90 j
Le SOPK peut être associé à l’hypertension. Une récente méta-analyse a montré que le risque d’hypertension était plus élevé seulement chez les personnes en âge de procréer (RR regroupé 1,72, intervalle de confiance [IC] de 95 % 1,43–2,07), et non chez les personnes ménopausées qui avaient souffert d’un SOPK durant leurs années de fertilité (RR regroupé 1,26, IC de 95 % 0,95–1,67)29. À ce titre, les personnes atteintes de SOPK devraient faire vérifier leur tension artérielle tous les ans et dès qu’elles souhaitent procréer, car elles sont exposées à un risque accru de troubles hypertensifs durant la grossesse1.
Les données quant au risque cardiovasculaire sont divergentes, même si cela est probablement dû au faible taux d’événements cardiovasculaires majeurs chez les femmes préménopausées28. Récemment, plusieurs méta-analyses ont laissé entendre sur la base de données de faible à très faible degré de certitude que les femmes atteintes de SOPK ont des rapports des cotes (RC) ou des ratios de taux d’incidence plus élevés à l’égard de plusieurs paramètres tels que maladie cardiovasculaire mixte, maladie cardiaque ischémique mixte, infarctus du myocarde, AVC et mortalité cardiovasculaire1. Ainsi, la surveillance du profil de risque cardiovasculaire, incluant des bilans lipidiques, est nécessaire au départ et de façon continue chez toutes les personnes atteintes de SOPK1.
Le syndrome des ovaires polykystiques est aussi lié à l’hyperinsulinémie, à l’intolérance au glucose et au diabète de type 29,16,22. Une méta-analyse regroupant 41 études a fait état d’un risque accru de diabète de type 2 chez les personnes atteintes de SOPK comparativement aux personnes indemnes (RC de 2,87, IC de 95 % 1,37–6,01)1. L’hyperinsulinémie est présente chez 75 % des personnes atteintes de SOPK qui ont un IMC de 25 ou moins et chez 95 % de celles qui ont un IMC supérieur à 251.
Le SOPK est associé à un risque plus élevé d’apnée obstructive du sommeil, indépendamment de l’IMC. Dans une récente méta-analyse de 8 études, les personnes atteintes de SOPK étaient 10 fois plus à risque à l’égard de l’apnée obstructive du sommeil que les personnes indemnes, avec un rapport des cotes (RC) de 9,52 (IC de 95 %, 3,90–23,26)3. Les personnes atteintes de SOPK devraient faire l’objet d’un dépistage de l’apnée obstructive du sommeil au moyen d’outils appropriés (p. ex., questionnaire de Berlin) et être orientées vers un dépistage, et le cas échéant, un traitement de l’apnée obstructive du sommeil3.
La dépression et l’anxiété ont aussi une forte prévalence chez les personnes atteintes de SOPK. Dans une méta-analyse de 47 études, la dépression était plus probable chez les personnes atteintes de SOPK que chez les personnes indemnes (RC 2,59, IC de 95 % 2,11–3,16)1. Dans une méta-analyse de 27 études sur l’anxiété, les personnes atteintes de SOPK avaient un risque plus élevé d’anxiété que les personnes indemnes, avec un RC de 2,68 (IC de 95 % 2,08–3,44)1. Le SOPK peut avoir des incidences négatives sur l’image corporelle et l’estime de soi et est aussi associé à un taux plus élevé de troubles alimentaires1.
Conclusion
Le SOPK, un problème endocrinien répandu chez les femmes en âge de procréer, s’accompagne de cycles menstruels irréguliers, d’hyperandrogénie et d’une morphologie ovarienne polykystique. Il est associé à d’importantes complications médicales à long terme, comme l’hypertension, le risque de cancers, et des problèmes métaboliques, cardiaques, psychologiques et de fertilité. Un diagnostic précoce permet d’améliorer les symptômes et de prévenir les complications à long terme.
Footnotes
Intérêts concurrents: Mara Sobel déclare avoir reçu des honoraires de la société Bayer. Aucun autre intérêt concurrent n’a été déclaré. Cet article a été révisé par des pairs.
Collaboratrices: Toutes les autrices ont contribué à l’élaboration et à la conception de l’étude, ont rédigé le manuscrit et en ont révisé de façon critique le contenu intellectuel important; elles ont donné leur approbation finale pour la version destinée à être publiée et assument l’entière responsabilité de tous les aspects du travail.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/