L’hémorragie majeure est un problème clinique complexe qui peut accompagner les traumatismes, les saignements post-partum, les grandes chirurgies et les hémorragies digestives.
Un protocole d’hémorragie massive (PHM) doit être déclenché quand l’hémorragie n’est pas maîtrisée, qu’elle répond à des critères précis et qu’elle est susceptible de justifier l’administration de plusieurs produits sanguins, en plus des culots globulaires.
L’acide tranexamique doit être envisagé dans les cas d’hémorragie majeure.
Lorsqu’un PHM est déclenché, il faut administrer le plasma selon un rapport de 2 culots globulaires pour 1 unité de plasma; les transfusions de plasma dépendent par la suite des résultats des analyses hémostatiques.
Les transfusions de plaquettes et l’administration de fibrinogène dépendent des résultats des analyses de laboratoire.
Les analyses de laboratoire doivent être répétées toutes les heures pendant la réanimation pour guider l’administration des produits sanguins en fonction de cibles précises.
L’hémorragie majeure menace le pronostic vital et peut survenir dans divers contextes cliniques. Aux fins de la présente revue, nous avons défini l’hémorragie majeure comme un saignement menaçant le pronostic vital et susceptible de justifier une transfusion massive (c.-à-d., ≥ 10 culots globulaires en 24 heures)1,2. Nous n’en avons pas utilisé la définition courante de la Société internationale de thrombose et d’hémostase parce que certains épisodes hémorragiques cités ne justifient pas de transfusions (p. ex., saignements intraoculaires ou intra-articulaires, baisse de 20 g/L du taux d’hémoglobine)3. La prise en charge de l’hémorragie majeure est plus complexe en milieu rural où l’accès aux produits sanguins et aux analyses de laboratoire spécialisées est limité. Face à une hémorragie majeure, il faut rapidement mobiliser toute une équipe multidisciplinaire.
Pour l’hémorragie majeure, les pratiques optimales s’appuient désormais sur plusieurs essais randomisés contrôlés (ERC), comme le montre le tableau 1; ces ERC ont mené à la création de protocoles d’hémorragie massive (PHM) standardisés. Mais les PHM n’ont toutefois pas été simples à déployer et à respecter. Nous passons en revue les données probantes concernant la prise en charge de l’hémorragie majeure et les PHM afin d’en soutenir le déploiement dans tous les types d’hôpitaux et d’optimiser ainsi les soins (encadré 1)17,18.
Principaux essais randomisés contrôlés pour guider la prise en charge clinique des hémorragies majeures
Encadré 1 : Recherche documentaire
Nous avons interrogé le réseau PubMed de janvier 2010 à décembre 2022 pour y recenser les grands essais randomisés contrôlés (> 100 sujets) sur l’hémorragie majeure secondaire à des traumatismes, des complications de la grossesse, des hémorragies digestives ou des interventions chirurgicales. Nous avons aussi inclus des revues systématiques pertinentes regroupant des essais randomisés et les lignes directrices publiées sur la prise en charge de l’hémorragie majeure dans de tels contextes.
Qu’est-ce qu’un protocole d’hémorragie massive?
Un PHM est une approche standardisée, fondée sur des données probantes, pour la prise en charge de l’hémorragie majeure. Le protocole définit les critères/seuils et le processus d’activation (téléphonique ou électronique), explique la façon de se procurer les produits (p. ex., autorisation automatique de plusieurs unités), précise le type et la fréquence des analyses de laboratoire, ainsi que les critères/seuils pour l’administration des transfusions et de l’acide tranexamique (TXA) et les critères d’arrêt du PHM. Un PHM devrait être en place dans tous les établissements qui maintiennent des stocks de culots globulaires, ou qui ont un service des urgences, une unité de soins intensifs, une salle d’accouchement ou un bloc opératoire19. La maîtrise rapide de la source de l’hémorragie, la mise en place d’un double accès veineux (de calibre 18 ou plus) et le recours possible à une hypotension permissive jusqu’à ce que l’on ait maîtrisé l’hémorragie à sa source dans certains cas (p. ex., blessure pénétrante en l’absence de traumatisme crânien)20 en sont des éléments cruciaux. Le PHM doit être conçu de manière à réduire le nombre d’appels téléphoniques à la banque de sang qui interrompent et retardent le travail des technologues en immunohématologie (épreuves de compatibilité croisée, décongélation du plasma et préparation des concentrés de fibrinogène). Une piètre observance du PHM est associée à une issue moins favorable17,19. L’administration rigoureuse des transfusions sanguines contribuerait à compenser la coagulopathie aiguë traumatique à l’origine de l’hypofibrinogénémie profonde21.
Quand faut-il déclencher le protocole d’hémorragie massive?
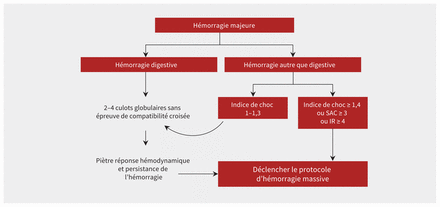
Il faut déclencher un PHM dans les cas d’hémorragie non maîtrisée qui présentent les critères cliniques établis par l’établissement local et risquent de nécessiter d’autres produits sanguins en plus de culots globulaires. Face à une hémorragie, l’équipe clinique doit décider si elle déclenche le PHM ou si elle demande plutôt un à la fois les différents produits sanguins requis (p. ex., 2 à 4 culots globulaires sans épreuve de compatibilité croisée). Tout recours indu au PHM impose un fardeau majeur au personnel des banques de sang et diminue les stocks de produits sanguins, entraînant ainsi plus de gaspillage. Les épisodes hémorragiques ne sont pas tous suffisamment graves pour justifier une transfusion sanguine, il est alors approprié d’amorcer la réanimation à l’aide de cristalloïdes seuls. Certains experts ont suggéré d’administrer 2 unités de sang sans épreuve de compatibilité croisée avant d’instaurer le PHM pour atténuer les effets d’un recours injustifié à ce dernier22.
Aucun critère ou seuil hémorragique à partir desquels il faut déclencher le PHM ne fait consensus. Une revue systématique a permis de recenser 24 outils potentiels de prédiction du recours au PHM23. Plusieurs ne s’appliquent qu’en traumatologie, reposent sur plusieurs variables ou requièrent des calculs complexes, mais chez les polytraumatisés, un indice de choc (fréquence cardiaque divisée par tension artérielle systolique) supérieur à 1 est plus sensible que les scores de traumatologie plus complexes (p. ex., score d’utilisation des produits sanguins) et s’applique facilement à la plupart des cas d’hémorragie24. Les autres options évaluées en traumatologie incluent le score du seuil d’administration critique (SAC) ou le score d’intensité de la réanimation (IR)25. Un score SAC de 3 ou plus (SAC3+) se définit par la transfusion de 3 culots globulaires ou plus au cours de la première heure de la réanimation. Un score IR de 4 ou plus (IR4+) se définit par l’administration de 4 ou plus de l’un ou l’autre des éléments suivants au cours des 30 premières minutes : unités de sang (culots globulaires, unités de plasma ou de plaquettes), 500 mL de colloïdes ou 1000 mL de cristalloïdes.
Aucun outil pour le déclenchement du PHM n’a été validé sauf en traumatologie. On déconseille le PHN pour l’hémorragie digestive, dont la prise en charge repose habituellement sur l’administration de cristalloïdes ou de culots globulaires seulement. Dans un ensemble d’ERC sur l’administration de culots globulaires pour l’hémorragie digestive au Royaume-Uni (essai TRIGGER), seulement 5 % environ des 936 sujets inscrits ont eu besoin de suppléments de plasma, de plaquettes ou de fibrinogène26.
Tous les hôpitaux doivent se doter de politiques d’autorisation rapide des culots globulaires du groupe O sans épreuve de compatibilité croisée. Un algorithme décisionnel suggéré pour le déclenchement du protocole est présenté à la figure 1.
Algorithme pour le déclenchement d’un protocole d’hémorragie massive en cas d’hémorragie majeure. Un score du seuil d’administration critique (SAC) de 3 ou plus (SAC3+) se définit par la transfusion de 3 culots globulaires ou plus au cours de la première heure de la réanimation. Un score d’intensité de la réanimation (IR) de 4 ou plus (IR4+) se définit par le recours à 4 ou plus de l’un ou l’autre des éléments suivants au cours des 30 premières minutes : unités de sang (culots globulaires, unités de plasma ou de plaquettes), 500 mL de colloïdes ou 1000 mL de cristalloïdes. L’indice de choc est calculé comme suit : fréquence cardiaque divisée par tension artérielle systolique.
Qui devrait recevoir de l’acide tranexamique?
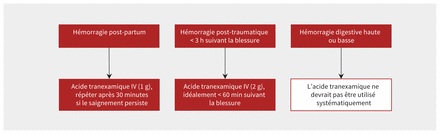
L’acide tranexamique (TXA) pour l’hémorragie majeure a fait l’objet d’études approfondies (tableau 1). Dans la plupart des cas, il faut l’administrer le plus tôt possible après le déclenchement de l’hémorragie, à l’exception de l’hémorragie digestive pour laquelle on n’en a démontré aucun avantage. La figure 2 présente une approche suggérée. Lors de l’étude CRASH-2 (Clinical Randomisation of an Antifibrinolytic in Significant Haemorrhage 2), des cas de traumatologie ont été assignés aléatoirement, soit au TXA (1 g en bolus puis 1 g en perfusion sur une période de 8 heures), soit à un placebo4. L’acide tranexamique a réduit le risque de mortalité de toutes causes et de mortalité hémorragique sans faire augmenter les complications thromboemboliques. Un bienfait a été observé uniquement chez les personnes ayant reçu le médicament dans les 3 heures suivant le traumatisme, et ce bienfait était plus prononcé si l’agent avait été administré dans les 60 minutes (risque relatif [RR] de décès 0,68, intervalle de confiance [IC] de 95 % 0,57–0,82). Lors de l’étude STAAMP (Study of Tranexamic Acid during Air Medical and Ground Prehospital Transport), des cas de traumatologie ont été assignés aléatoirement, soit à 1 g de TXA, soit à un placebo avant d’arriver à l’hôpital9. Puis, à leur arrivée à l’hôpital les cas traités par TXA ont été assignés, soit à un placebo, soit à 1 ou à 2 g de TXA. La réduction la plus marquée du taux de mortalité à 30 jours a été observée dans les sous-groupes traités dans les 60 minutes suivant le traumatisme, ayant reçu une dose totale de 3 g de TXA ou en choc grave (tension artérielle systolique < 70 mm Hg). Afin de simplifier les soins, plusieurs programmes de traumatologie administrent désormais 2 g de TXA en bolus le plus tôt possible après le traumatisme, sur la base des résultats de l’essai STAAMP et d’un essai sur les traumatismes crâniens au cours duquel 2 g de TXA ont été administrés en perfusion rapide sans danger avant l’arrivée à l’hôpital9,27. Le TXA préhospitalier est de plus en plus utilisé dans le monde et est associé à des taux moindres de transfusion et de mortalité lorsqu’il fait partie d’une norme de soins28,29.
Utilisation de l’acide tranexamique pour l’hémorragie majeure. Remarque : IV = par voie intraveineuse.
Lors de l’essai WOMAN (World Maternal Antifibrinolytic), des femmes en hémorragie post-partum ont été affectées aléatoirement soit au TXA (1 g en bolus, répété au bout de 30 minutes si le saignement continuait) ou à un placebo5. L’acide tranexamique a réduit le risque de mortalité par hémorragie obstétricale (RR 0,81, IC de 95 % 0,65–1,00), surtout s’il était administré dans les 3 heures suivant le début du saignement (RR 0,69, IC de 95 % 0,52–0,91).
En revanche, l’essai HALT-IT (Haemorrhage Alleviation with Tranexamic Acid — Intestinal System), sur de graves cas d’hémorragie digestive haute et basse, a fait état d’une absence d’amélioration du risque de mortalité par hémorragie digestive liée à l’administration de TXA (RR 0,99, IC de 95 % 0,82–1,18) et d’un risque accru de complications thromboemboliques veineuses (RR 1,85, IC de 95 % 1,15–2,98). Lors de cet essai, les groupes étaient assignés aléatoirement, soit à 4 g (1 g en bolus et 3 g en perfusion sur 24 h) de TXA, soit à un placebo6. Le risque accru de thromboembolie peut avoir découlé de la dose importante utilisée, de la durée prolongée de la perfusion, de l’âge plus avancé des sujets ou de l’inclusion de cas de cirrhose sous hémostase corrigée. L’absence de bienfaits observés peut s’expliquer par la nécessité d’administrer le TXA peu de temps après le début de l’hémorragie digestive, alors qu’il arrive souvent que cette dernière ne soit reconnue qu’après plusieurs heures. L’essai a recruté surtout des cas d’hémorragie digestive haute non massive et les délais d’intervention ont grandement varié.
L’acide tranexamique a fait l’objet de nombreuses études en prévention, mais non en traitement de l’hémorragie périopératoire. Une revue systématique a permis de recenser 129 ERC regroupant 10 488 cas de chirurgie30. L’acide tranexamique a réduit le recours à la transfusion (RR 0,62, IC de 95 % 0,58–0,65) sans accroître le risque de complications thromboemboliques. Par la suite, l’essai POISE-3 (Perioperative Ischemic Evaluation-3), regroupant 9535 cas randomisés, a démontré que 1 g de TXA au début et à la fin de la chirurgie réduisait le risque d’hémorragie majeure comparativement au placebo (RR 0,72, IC de 95 % 0,63–0,83)8. De même, l’essai ATACAS (Aspirin and Tranexamic Acid for Coronary ArterySurgery), qui incluait 4662 cas de chirurgie cardiaque, a révélé que le TXA (50 mg/kg) réduisait le risque de transfusion (37,9 % c. 54,7 %, p < 0,001) et de réintervention pour hémorragie (RR 0,49, IC de 95 % 0,32–0,75), comparativement au placebo7.
Le cas échéant, quels produits sanguins faut-il administrer avant même d’obtenir les résultats d’analyses de laboratoire?
Lorsque les critères de déclenchement du PHM sont en place, les transfusions de plasma doivent commencer selon un rapport minimum de 2 culots globulaires par unité de plasma et tous les autres éléments sont administrés en fonction des résultats des analyses hémostatiques. Un ERC regroupant 680 cas de traumatologie a comparé les rapports 1:1:1 et 2:1:1 pour les culots globulaires, les unités de plasma et de plaquettes et n’a fait état d’aucune amélioration du taux de mortalité après 24 heures et 30 jours, ou du nombre de jours hors de l’unité des soins intensifs ou hors de l’hôpital avec le schéma 1:1:115.
Aucun ERC sur la réanimation portant sur les rapports entre les différents éléments sanguins n’a été effectué sauf en traumatologie. Une étude observationnelle regroupant 865 situations de transfusion massive n’a fait état d’aucune amélioration des résultats entre les deux types de rapports31. Les lignes directrices de la Société européenne de médecine de soins intensifs32, de la Société britannique d’hématologie33 et du Groupe de travail multidisciplinaire paneuropéen sur les soins hémostatiques avancés en traumatologie34 recommandent une réanimation initiale selon un rapport de 2 culots globulaires par unité de plasma.
Ce rapport fixe est indiqué uniquement pendant les 30 à 60 premières minutes de réanimation et doit ensuite laisser place à une prise en charge fondée sur des cibles, selon les résultats de fréquentes analyses de laboratoire (notamment les taux d’hémoglobine, de plaquettes et de fibrinogène et le ratio international normalisé [RIN]). Cela prévient les transfusions superflues et permet d’éviter une coagulopathie non traitée. La numération plaquettaire ne diminue habituellement pas sous les seuils transfusionnels durant le PHM (elle ne baissera à moins de 100 × 109/L au cours des 24 premières heures que chez 40 % des sujets)35,36.
Quel type de surveillance faut-il exercer pour s’assurer d’atteindre les cibles appropriées?
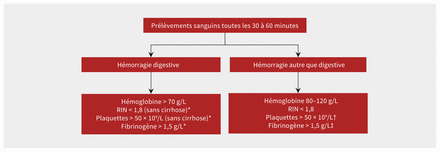
On répétera les analyses de laboratoire pour pouvoir administrer les transfusions en fonction des cibles fixées, corriger les dérèglements hémostatiques et surveiller les complications des transfusions massives. Il faut au départ établir les taux d’hémoglobine, de plaquettes, de fibrinogène, de potassium et de calcium, le RIN, les gaz veineux pour le pH et l’excès de base et le lactate. La ligne directrice de la Société britannique d’hématologie recommande d’effectuer ces analyses toutes les 30 à 60 minutes pendant l’hémorragie active pour éviter d’administrer trop ou trop peu de transfusions33. Dans la mesure du possible, les résultats des analyses hématologiques et hémostatiques, normales et anormales, sont transmis directement à l’équipe clinique. Il est important de suivre l’hypocalcémie due à la toxicité du citrate des éléments sanguins et l’hyperkaliémie due à la perfusion rapide des culots globulaires, l’accumulation de sang entraînant une hausse des taux de potassium avec le temps. La figure 3 donne une idée des cibles à viser pour les analyses de laboratoire durant la réanimation.
Fréquence des analyses de laboratoire et cibles hémostatiques. *Aucune cible n’est suggérée en présence de cirrhose. †Plus de 100 × 109/L en cas de traumatisme crânien. ‡Plus de 2,0 g/L en cas d’hémorragie post-partum. Remarque : RIN = ratio international normalisé.
On ne dispose d’aucune donnée provenant d’essais cliniques quant à un seuil d’hémoglobine cible pour l’hémorragie majeure, mais pour l’hémorragie digestive haute aiguë non majeure, une stratégie limitant les transfusions a amélioré les résultats. Dans un ERC regroupant 921 cas d’hémorragie digestive haute aiguë qui comparait un seuil d’hémoglobine de 70 g/L (cible post-transfusionnelle de 70–90 g/L) et un seuil de 90 g/L (cible post-transfusionnelle de 90–110 g/L), le groupe soumis au seuil restrictif a reçu un nombre et un volume moindres (49 % c. 86 %, moyenne 1,5 c. 3,7 unités, respectivement), a connu moins de reprises des saignements et moins d’effets indésirables et présenté un risque de mortalité plus bas (rapport de risque [HR pour hazard ratio] 0,55, IC de 95 % 0,33–0,92)16. Une revue systématique incluant 5 ERC et un total de 1965 cas a révélé que la stratégie restrictive avait amélioré le taux de mortalité de toutes causes (RR 0,65, IC de 95 % 0,44–0,97)37. Des seuils d’hémoglobine plus élevés entraîneraient plus de reprises des saignements et des taux de mortalité en hausse parce que les transfusions augmentent la pression portale. La ligne directrice du Collège américain de gastroentérologie recommande de toujours limiter les transfusions à un seuil de 70 g/L pour l’hémorragie digestive haute aiguë38.
Certains ERC ont comparé des seuils libéraux à des seuils plus restrictifs lors de divers types d’interventions chirurgicales. On n’a observé aucun avantage lié à une stratégie de transfusion libérale, même si on ignore la proportion exacte des hémorragies majeures et le niveau de conformité aux seuils fixés pour ces essais39. Une revue rétrospective de 418 cas de traumatologie traités par transfusions massives dans un seul centre a révélé que les taux d’hémoglobine 24 heures après la réanimation permettaient de prédire le risque de mortalité40. Les transfusions en fonction d’un seuil d’hémoglobine inférieur à 80 g/L ont été associées à un risque accru de décès (rapport des cotes [RC] 3,3, IC de 95 % 1,6–6,7), tout comme les transfusions en fonction d’un seuil supérieur à 120 g/L (RC 2,5, IC de 95 % 1,1–5,6). Étant donné l’absence de données concluantes, il est prudent de mesurer l’hémoglobine tout au long de la réanimation afin d’éviter les conséquences d’une quantité insuffisante ou excessive de transfusions (p. ex., hypoperfusion des organes, coagulopathie liée à l’anémie, surcharge liquidienne)41. Les paramètres cibles de la figure 3 visent le maintien d’un taux d’hémoglobine supérieur à 60 g/L durant la réanimation et la réduction du nombre de transfusions superflues, définies par un taux d’hémoglobine supérieur à 110 g/L 24 heures après l’épisode hémorragique19.
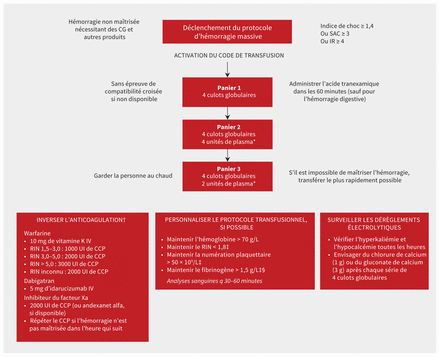
Comme pour l’hémoglobine, aucune donnée tirée d’essais cliniques ne privilégie un seuil de RIN particulier pour guider les transfusions de plasma. Plusieurs facteurs expliquent la hausse du RIN lors d’une hémorragie majeure, notamment, la coagulopathie liée au choc ou au traumatisme, le traumatisme crânien et la dilution des facteurs de la coagulation par les liquides de réanimation. Le Groupe de travail multidisciplinaire sur les soins hémostatiques avancés en traumatologie recommande le maintien d’un temps de prothrombine inférieur à 1,5 fois la normale ou la surveillance des signes viscoélastiques des troubles de l’hémostase34. Une ligne directrice spécifique aux cas de cirrhose publiée par l’Association européenne pour l’étude du foie (AEEF) précise qu’en l’absence de données probantes pour appuyer la correction des dérèglements hémostatiques, on évitera toute tentative de contrer la coagulopathie au moyen du plasma en raison du risque de surcharge liquidienne et d’aggravation de l’hypertension portale42. En terminant, selon la ligne directrice de 2022 Baveno VII sur la prise en charge de l’hémorragie sur fond d’hypertension portale, « la transfusion de plasma frais congelé n’est pas recommandée puisqu’elle ne corrigera pas la coagulopathie et pourrait entraîner une surcharge volémique et l’aggravation de l’hypertension portale »43. Étant donné que le plasma a un volume élevé (15 mL/kg ou 1000 mL par dose), que le RIN n’est pas en corrélation avec les paramètres hémostatiques en présence de cirrhose et que le plasma peut accroître la pression portale et donc, le risque de reprise des saignements, l’administration de plasma devrait être rare, voire nulle, en présence de cirrhose. En raison de l’absence de répercussions du plasma sur le RIN lorsqu’il est à un taux inférieur à 1,8, il est raisonnable d’administrer du plasma pour atteindre ce seuil en cas d’hémorragie majeure, en l’absence de cirrhose avec un RIN supérieur à 1,844.
Aucun ERC n’a comparé les différents seuils transfusionnels pour les plaquettes lors d’une hémorragie majeure. La ligne directrice de la Société britannique d’hématologie recommande le maintien d’une numération plaquettaire supérieure à 50 × 109/L33. Le Groupe de travail multidisciplinaire sur les soins hémostatiques avancés en traumatologie recommande le maintien d’une numération plaquettaire supérieure à 50 × 109/L dans tous les cas et supérieure à 100 × 109/L dans les cas de traumatisme crânien34; nous suggérons d’observer ces lignes directrices (figure 3) à l’exception des cas de cirrhose pour lesquels les transfusions plaquettaires peuvent être envisagées si les saignements ne sont pas maîtrisés par le biais d’interventions locales43. En présence d’hémorragie majeure chez des malades sous antiplaquettaires, il faut probablement éviter les transfusions de plaquettes, compte tenu des risques ou de l’absence de bienfaits cliniques, sauf en chirurgie cardiaque45–50.
Des essais regroupant des victimes d’hémorragie majeure ont comparé les épreuves de laboratoire classiques (p. ex., RIN, fibrinogène) aux tests de viscoélasticité (p. ex., thromboélastographie, thromboélastométrie rotationnelle) en chirurgie cardiaque, en traumatologie et dans les cas d’hémorragie digestive. Les tests de viscoélasticité se font en contexte clinique sur du sang entier et permettent d’ajuster les quantités de plasma, de plaquettes et de fibrinogène à administrer. Un essai randomisé multicentrique par grappes et par étapes a comparé les analyses de laboratoire classiques aux tests de viscoélasticité dans 7402 cas de chirurgie cardiaque51; il a révélé que l’utilisation des tests de viscoélasticité réduisait le risque de transfusion et d’hémorragie majeure. En revanche, un ERC regroupant 396 cas de polytraumatologie n’a fait état d’aucun avantage des tests de viscoélasticité chez ces sujets13. En ce qui concerne l’hémorragie digestive aiguë sur fond de cirrhose (pour laquelle il est rare qu’on transfuse massivement), 2 essais (n = 96 et n = 60) ont comparé les analyses de laboratoire classiques aux tests de viscoélasticité et ont constaté des taux significativement moindres de transfusion et des taux similaires de maîtrise des saignements lorsque les transfusions étaient guidées par les tests de viscoélasticité52,53. Les lignes directrices de 2022 de l’AEEF pour la prise en charge de l’hémorragie en présence de cirrhose recommandent un recours aux tests de viscoélasticité42. L’utilisation des tests de viscoélasticité est de plus en plus courante, mais n’est pas facilement accessible à l’extérieur des centres de soins tertiaires au Canada54.
Quand faut-il administrer des concentrés de fibrinogène ou de complexe prothrombique?
Selon les lignes directrices, il faut maintenir des taux de fibrinogène supérieurs à 1,5 g/L (> 2,0 g/L pour l’hémorragie post-partum) au moyen d’un concentré de fibrinogène32–34. Le concentré de fibrinogène a remplacé les cryoprécipités dans la plupart des régions du Canada en raison de son équivalence au plan hémostatique et de sa meilleure innocuité55. Aucun ERC concluant n’a été réalisé pour comparer des seuils plus ou moins élevés à partir desquels instaurer un traitement par fibrinogène. L’ERC CRYOSTAT-2 (NCT047004869) a recruté 1568 victimes de traumatisme majeur pour qui un PHM a été déclenché et qui ont été assignées aléatoirement, soit à 15 unités de cryoprécipités (4–6 g de fibrinogène), soit aux soins standard56. Les résultats sont prévus pour 2023 et permettront de clarifier si un traitement hâtif par fibrinogène permet de réduire le risque de mortalité en polytraumatologie.
Le concentré de complexe prothrombique (CCP) est un concentré viroatténué de facteurs II, VII, IX et X de faible volume (40 mL par dose de 1000 UI). Le produit est actuellement utilisé principalement comme agent d’inversion de la warfarine lors d’hémorragies menaçant le pronostic vital ou d’interventions médicales urgentes qui ne peuvent pas être retardées de 6 heures pour attendre que la vitamine K intraveineuse agisse. L’inversion du traitement anticoagulant au moyen du CCP n’est pas recommandée pour l’hémorragie digestive, sauf peut-être si elle menace le pronostic vital45,46. Son utilisation comme solution de rechange au plasma fait l’objet d’études dans plusieurs ERC prospectifs (NCT03218722, NCT04534751, NCT05523297)57. L’efficacité hémostatique du CCP semble similaire à celle du plasma selon des ERC pilotes58,59. L’utilisation du CCP en association avec le fibrinogène en attente d’un transfert vers un hôpital ayant de meilleures capacités transfusionnelles est une stratégie envisageable pour les établissements des régions rurales qui ne peuvent pas préparer le plasma19,60.
La figure 4 présente un algorithme suggéré pour chacun des éléments d’un PHM, y compris l’inversion de l’anticoagulation. On trouvera d’autres renseignements sur l’inversion des agents anticoagulants en cas d’hémorragie majeure dans les lignes directrices récentes et complètes45,61. Le tableau 2 propose des modifications au PHM adaptées à différentes populations.
Algorithme pour un protocole d’hémorragie massive générique en cas d’hémorragie majeure. Un score du seuil d’administration critique (SAC) de 3 ou plus (SAC3+) se définit par la transfusion de 3 culots globulaires ou plus au cours de la première heure de la réanimation. Un score d’intensité de la réanimation (IR) de 4 ou plus (IR4+) se définit par le recours à 4 ou plus de l’un ou l’autre des éléments suivants au cours des 30 premières minutes : unités de sang (culots globulaires, unités de plasma ou de plaquettes), 500 mL de colloïdes ou 1000 mL de cristalloïdes. L’indice de choc est calculé comme suit : fréquence cardiaque divisée par tension artérielle systolique. *En milieu rural, si le plasma n’est pas disponible, envisager 2000 UI de concentré de complexe prothrombique (CCP) et 4 g de fibrinogène; éviter le plasma en présence de cirrhose. †L’inversion n’est pas recommandée pour l’hémorragie digestive à moins qu’elle ne menace le pronostic vital. ‡Aucune cible n’est suggérée en présence de cirrhose. §> 2,0 g/L pour les hémorragies post-partum. Remarque : CG = culot globulaire, IV = par voie intraveineuse, RIN = ratio international normalisé.
Modifications des protocoles d’hémorragie massive selon certaines conditions
Conclusion
L’hémorragie majeure menace le pronostic vital et sa prise en charge est complexe, surtout en région rurale où l’accès aux produits sanguins et aux analyses de laboratoire spécialisées et la capacité de maîtriser les saignements sont parfois limités. Les protocoles d’hémorragie massive proposent une orientation fondée sur des données probantes et peuvent être adaptés selon la source de l’hémorragie et les caractéristiques propres à l’individu touché. L’administration rapide de TXA améliore les résultats, sauf en présence d’hémorragie digestive. Les questions en suspens auxquelles les futures recherches devront répondre sont présentées dans l’encadré 2.
Encadré 2 :
Questions sans réponsesLes transfusions préhospitalières améliorent-elles les résultats?
Le sang entier a-t-il un rôle à jouer dans la prise en charge initiale de l’hémorragie majeure?
Quel est la plateforme de laboratoire optimale (meilleur appareil) pour les analyses hémostatiques servant à guider les décisions transfusionnelles?
Quel est le rôle des concentrés de facteur de coagulation en cas d’hémorragie majeure?
Quelles sont les cibles appropriées de la réanimation pour l’hémoglobine, la numération plaquettaire et le ratio international normalisé et le fibrinogène en cas d’hémorragie majeure?
Comment les hôpitaux éloignés et ruraux devraient-ils gérer efficacement les cas d’hémorragie en attente d’un transfert pour une maîtrise définitive de l’hémorragie?
Footnotes
Intérêts concurrents: Jeannie Callum a reçu des subventions de recherche de la Société canadienne du sang (qui fabrique et distribue des produits sanguins) et de la société Octapharma (qui fabrique des concentrés de complexe prothrombique et de fibrinogène). Elle fait partie du comité des mises en candidature de l’Association pour l’avancement des traitements par le sang et des biothérapies et des comités de surveillance de la sécurité des données pour l’essai TRACE (Tranexamic Acid for Subdural Hematoma), une étude pilote de l’Université d’Ottawa sur l’acide tranexamique pour la thrombocytopénie hypoproliférative, et l’étude FEISTY (supplément de fibrinogène en traumatologie). Alan Barkun a reçu des honoraires de consultation des sociétés AstraZeneca et Medtronic. Keyvan Karkouti a reçu des subventions de recherche, des honoraires de consultation et autres de la société Octapharma et des honoraires de consultation de la société Werfen (qui fournit des tests de viscoélasticité en contexte clinique). Il fait partie de comités de révision des Instituts de recherche en santé du Canada et de la Fondation des maladies du cœur. Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Collaborateurs : Tous les auteurs ont contribué à la conception du travail, ont rédigé le manuscrit et en ont révisé de façon critique le contenu intellectuel important; ils ont donné leur approbation finale pour la version destinée à être publiée et assument l’entière responsabilité de tous les aspects du travail.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/